Proses ini sangat
penting dalam industri, karena senyawa – senyawa organik dengan gugus khlor
banyak sekali digunakan, antara lain : refrigerant (CCl2F2),
larutan pembersih (CHCl=CCl2), anestetik (CHCl3) serta senyawa
khloroparafin yang banyak digunakan sebagai bahan bakar sintesa: alkohol, alkyl
oksida, eter, amina dan sebagainya.
Pada proses
khlorinasi hidrokarbon dan khlorohidrokarbon, hal yang perlu diperhatikan
adalah :
1. Kecepatan reaksi khlorinasi subtitusi
hidrogen pada proses khlorinasi untuk karbon ikatan jenuh lebih tinggi
dibanding pada karbon ikatan tak jenuh.
2. Kecepatan reaksi khlorinasi subtitusi
hidrogen pada karbon jenuh lebih besar dibanding kecepatan adisi untuk ikatan
rangkap pada suhu tinggi, dan untuk suhu rendah adalah kebalikannnya.
3. Kecepatan reaksi khlorinasi adisi pada
ikatan rangkap lebih tinggi daripada reaksi subtitusi hidrogen pada karbon tak
jenuh.
4. Kecepatan reaksi subtitusi hidrogen α
untuk khlorinasi kira – kira sama dengan subtitusi hidrogen pada atom karbon
lain.
5. Kecepata reaksi subtitusi hidrogen β untuk
khlorinasi adalah lebih kecil daripada subtitusi hidrogen pada atom karbon
biasa.
6. Kecepatan reaksi subtitusi γ untuk
khlorinasi adalah sangat kecil dibanding subtitusi hidrogen pada atom karbon
biasa.
Reaksi khlorinasi
pada rantai karbon pada hidrokarbon parafin (alkana) bisa berupa rantai lurus
dan bercabang, sehingga atom C bisa bersifar primer, sekunder dan tersier.
Kecepatan reaksi khlorinasi subtitusi berurut sebagai berikut : primer <
sekunder < tersier. Bila rantai karbon semakin panjang maka hasil khlorinasi
semakin kompleks.
Khlorinasi Etanol
Bila alkohol
absolut dikhlorinasi akan terbentuk hemiasetal
Akan tetapi
alkohol yang mengandung air, yang
terbentuk trikhloroasetaldehid (khloral)
Khlorinasi pada senyawa aromatis
Bila mempunyai gugus alkyl maka subtitusi gugus alkyl pada
suhu 120 – 130 0C tanpa katalis.
Jika senyawa
aromatis tidak mempunyai gugus alkil, maka terjadi khlorinasi inti aromatis
yaitu benzena, reaksi terjadi pada fase cair (suhu rendah 30 – 40 0C)
harus menggunakan katalis, dengan hasil terbanyak monokhlorobenzen. Sedangkan
reaksi terjadi pada fase gas (suhu tinggi 400 – 500 0C) banyak
dihasilkan 1,3,5 trikhlorobenzen dan bila suhu diatas 500 0C terjadi
pirolisis terbentuknya karbon dan heksakhlorobenzen.
Reaksi adisi pada
hidrokarbon tak jenuh berlaku aturan Markownikoff, yaitu atom Cl akan bergabung
pada atom C tak jenuh yang lebih sedikit mengikat atom H dibanding dengan atom
C tak jenuh lainnya.
Dehidrokhlorinasi
Reaksi ini
biasanya berlangsung secara thermal atau penggunaan katalis.
Contoh :




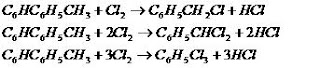

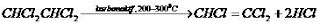












COMMENTS