Reaksi halogenasi
adaalah reaksi yang terjadi pengikatan satu atau lebih atom halogen (F, Cl. Br,
I) pada senyawa organik.
Secara umum,
jenis reaksi yang terjadi :
1. Adisi
Contoh :
2. Subtitusi
Contoh :
3. Penggantian gugus (replacement)
Contoh :
Klorinasi
1. Reaksi langsung dengan gas khlorine
Contoh :
2. Reaksi dengan HCl
Contoh :
3. Reaksi dengan Natrium hypoklorit
4. Khlorinasi dengan phosgen (COCl2)
dan benzpotrikhlorida (C6H5CCl3)
5. Khlorinasi dengan thionylkhlorida (SOCl2)
Contoh :
6. Khlorinasi dengan sulfury khlorida (SO2Cl2)
7. Khlorinasi dengan phospor khlorida
Contoh :
8. Reaksi sandmeyer
Contoh :
9. Reaksi Gattermann
Contoh :
Brominasi
Reagen yang
digunakan bisa bromine, bromida, bromat dan garam alkali hipobromit. Br larut
dalam air, namun untuk mendapatkan konsentrasi tinggi harus menggunakan pelarut
KBr.
Iodinasi
Ikatan yang
terjadi antara C-I lebih lemah dibandingkan dengan C-Cl dan C-BR, sehingga
reaksi iodinasi perlu senyawa lain sebagai media.
Contoh :
Flourinasi
1. Gas flourin (F2)
Contoh :
2. Asam flourida (HF)
Contoh :
3. Garam alkali
Contoh ;
4. Senyawa Diazo
Contoh :
Pada reaksi
flourinasi, baik adisi maupun subtitusi menghasilkan panas yang sangat besar.
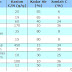
Secara umum
thermodinamika halogenisasi, energi ikatan makin menurun sesuai urutan
F-Cl-Br-I.
Pada reaksi
subtitusi bila dihubungkan dengan efek panasnya, maka sebagai berikut:
- Flourinasi sangat-sangat eksotermis
- Khlorinasi sangat eksotermis
- Brominasi eksotermis
- Iodinasi endotermis
Pada reaksi adisi
secara keseluruhan juga sangat eksotermis, sedangkan reaksi subtitusi adalah
endotermis.
TAGS :
adisi |
brominasi |
flourinasi |
Informasi |
klorinasi |
penggantian gugus |
reaksi halogenasi |
subtitusi |








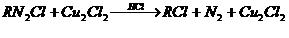


















COMMENTS